Природа
Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи , невалентном взаимодействии между атомом водорода H , ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR" . Результатом таких взаимодействий являются комплексы RA-H BR" различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR" .
Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность , её распространенность и важность, особенно в органических соединениях , а также некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода.
Свойства
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры . Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород , вода , аммиак .
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB) ± ; так, для комплекса (H 2 O H OH 2) + образованного H 2 O и H 3 O + - 132 кДж/моль в газовой фазе.
В воде
Механизм Гротгуса
В нуклеиновых кислотах и белках
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты . В частности, элементы вторичной структуры (например, α-спирали , β-складки) и третичной структуры в молекулах белков , РНК и ДНК стабилизированы водородными связями. В этих макромолекулах, водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определенную форму. Например, двойная спиральная структура ДНК, определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
В полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример - нейлон , где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина , хлопок и лён .
См. также
Примечания
Литература
- Химическая Энциклопедия. Советская Энциклопедия, М., 1988
- В. В. Москва. Водородная связь в органической химии. Соросовский образовательный журнал, 11999,N 2, с.58-64
| Химическая связь | |||||||
|---|---|---|---|---|---|---|---|
|
|||||||
| Межмолекулярное взаимодействие |
|||||||
Wikimedia Foundation . 2010 .
Между атомами водорода и атомом элемента, обладающим высокой электроотрицательностью, возникает особый тип связи - водородная химическая связь. Она может образовываться не только внутри молекулы, но и между соседними молекулами.
Общее описание
Электроотрицательность - способность атома удерживать валентные электроны на внешнем энергетическом уровне или количественная характеристика, показывающая, с какой силой притягиваются электроны к ядру атома. Наиболее электроотрицательными элементами являются фтор, азот и кислород.

Рис. 1. Ряд электроотрицательности.
Сильное электростатическое взаимодействие между атомом водорода и электроотрицательными атомами обуславливается небольшими размерами атома водорода и силой притяжения атомов элементов. В результате возникает частный случай ковалентной полярной связи. Примерами водородной химической связи являются:
- плавиковая кислота (HF);
- вода (H 2 O);
- аммиак (NH 3);
- соляная кислота (HCl);
- сероводород (H 2 S).
Наличие водородной связи обуславливает физические и химические свойства вещества. В частности определяет температуру плавления, кипения, растворимость, кислотность.
Особенностью связи является её невысокая прочность и распространённость, особенно в органических веществах.
Типы
Водородная связь бывают двух типов:
- межмолекулярная , возникающая между несколькими однотипными молекулами;
- внутримолекулярная , возникающая внутри одной молекулы.
Способ образования связи в обоих типах одинаковый. Разница только в том, что с помощью межмолекулярной водородной связи образуются цепочка молекул, а при внутримолекулярной связи водород «сцепляется» с атомами внутри молекулы.
Например, молекула воды образована одним атомом кислорода и двумя атомами водорода. За счёт высокой электроотрицательности кислород, на внешнем энергетическом уровне которого шесть электронов, притягивает единственные электроны двух атомов водорода. Две пары электронов кислорода остаются свободными. При этом у водорода освобождается орбиталь. Другая аналогичная молекула может присоединиться в месте свободных электронных пар атома кислорода, заполнив освободившуюся орбиталь водорода. Возникает межмолекулярная водородная связь.

Рис. 2. Строение молекулы воды.
Аналогичным образом соединяются молекулы плавиковой кислоты и аммиака. Однако связь между азотом и водородом будет слабее, чем между водородом и кислородом. Также молекулы плавиковой кислоты сильнее притягиваются друг к другу, чем молекулы воды. Это объясняется величиной электроотрицательности.
Внутримолекулярная водородная связь чаще всего возникает внутри сложных молекул органических веществ - белков, ДНК, аренов. Например, водородная связь образуется в молекуле салициловой кислоты между атомом водорода гидроксильной группы и кислорода, входящего в функциональную группу -СООН.

Рис. 3. Водородная связь в салициловой кислоте.
Водородные связи графически изображаются точками.
Что мы узнали?
Между атомами водорода и атомами неметаллов возникает водородная связь, основанная на электростатическом взаимодействии атомов. Это частный случай ковалентной полярной связи, характеризующийся взаимодействием водорода и атомов с высокой электроотрицательностью. Связь бывает двух типов: межмолекулярная, возникающая между молекулами вещества, и внутримолекулярная, возникающая между водородом и атомом другого элемента в одной молекуле. Водородная связь присуща неорганическим и органическим веществам.
Тест по теме
Оценка доклада
Средняя оценка: 4.5 . Всего получено оценок: 254.
Понятие водородная связь
Атом водорода, связанный с сильно электроотрицательным атомом (кислорода, фтора, хлора, азота) может взаимодействовать с неподеленной электронной парой другого сильно электроотрицательного атома этой или другой молекулы с образованием слабой дополнительной связи -- водородной связью. При этом может установиться равновесие
Рисунок 1.
Появление водородной связи предопределено исключительностью атома водорода. Атом водорода гораздо меньше, чем другие атомы. Электронное облако, образованное им и электроотрицательным атомом сильно смещено в сторону последнего. В результате ядро водорода остается слабоэкранированным.
Атомы кислорода гидроксильных групп двух молекул карбоновых кислот, спиртов или фенолов могут близко сходиться из-за образования водородных связей.
Положительный заряд ядра атома водорода и отрицательный заряд другого электроотрицательного атома притягиваются. Энергия их взаимодействия сопоставима с энергией прежней связи, поэтому протон оказывается связанным сразу с двумя атомами. Связь со вторым электроотрицательным атомом может быть более сильной, чем первоначальная связь.
Протон может передвигаться от одного электроотрицательного атома к другому. Энергетический барьер у такого перехода незначительный.
Водородные связи относятся к числу химических связей средней силы, но, если таких связей много, то они способствуют образованию прочных димерных или полимерных структур.
Пример 1
Образование водородной связи в $\alpha $-спиральной структуре дезоксирибонуклеиновой кислоты, алмазоподобная структура кристаллического льда и др.
Положительный конец диполя в гидроксильной группе находится у атома водорода, поэтому через водород может формироваться связь с анионами или электроотрицательными атомами, содержащими неподеленные электронные пары.
Практически во всех других полярных группах положительный конец диполя расположен внутри молекулы и поэтому является трудно доступным для связывания. У карбоновых кислот $(R=RCO)$, спиртов $(R=Alk)$, фенолов $(R=Ar)$ положительный конец диполя $OH$ находится снаружи молекулы:
Примеры нахождения положительного конца диполя $C-O, S-O, P-O$ внутри молекулы:

Рисунок 2. Ацетон, диметилсульфоксид (ДМСО), гексаметилфосфортриамид (ГМФТА)
Так как стерические препятствия отсутствуют, водородная связь образуется легко. Ее сила, в основном определяется тем, что она преимущественно имеет ковалентный характер.
Обычно наличие водородной связи обозначают пунктирной линией между донором и акцептором, например, у спиртов
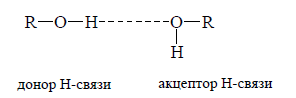
Рисунок 3.
Как правило, расстояние между двумя атомами кислорода и водородной связи меньше суммы ван-дер-ваальсовых радиусов атомов кислорода. Должно присутствовать взаимное отталкивание электронных оболочек атомов кислорода. Однако силы отталкивания преодолеваются силой водородной связи.
Природа водородной связи
Природа водородной связи заключается в электростатическом и донорно -- акцепторном характере. Основную роль в формировании энергии водородной связи играет электростатическое взаимодействие. В образовании межмолекулярной водородной связи принимают участие три атома, которые располагаются почти на одной прямой, но расстояния между ними, при этом, различны. (исключение составляет связь $F-H\cdots F-$).
Пример 2
Для межмолекулярных водородных связей во льду $-O-H\cdots OH_2$ расстояние $O-H$ равно $0,097$ нм, а расстояние $H\cdots O$ равно $0,179$ нм.
Энергия большинства водородных связей лежит в пределах $10-40$ кДж/моль, а это намного меньше энергии ковалентной или ионной связи. Часто можно наблюдать, что прочность водородных связей возрастает с увеличением кислотности донора и основности акцептора протона.
Значение межмолекулярной водородной связи
Водородная связь играет существенную роль в проявлениях физико -- химических свойств соединения.
Водородные связи оказывают следующее влияние на соединения:
Внутримолекулярные водородные связи
В случаях, когда возможно замыкание шестичленного или пятичленного цикла, образуются внутримолекулярные водородные связи.
Наличие внутримолекулярных водородных связей в салициловом альдегиде и о-нитрофеноле является причиной отличия их физических свойств от соответствующих мета- и пара- изомеров.
$o$-Гидроксибензальдегид или салициловый альдегид $(A)$ и $o$-нитрофенол (Б) не образуют межмолекулярные ассоциаты, поэтому имеют более низкие температуры кипения. Они плохо растворимы в воде, так как не участвуют в образовании межмолекулярных водородных связей с водой.

Рисунок 5.
$o$-Нитрофенол является единственным из трех изомерных представителей нитрофенолов, который способен перегоняться с водяным паром. На этом свойстве основано его выделение из смеси изомеров нитрофенола, которая образуется в результате нитрования фенолов.
Что такое водородная связь? Известный всем пример этой связи представляет обычная вода (H2O). Из-за того, что атом кислорода (О) более электроотрицателен, чем два атома водорода (Н), он как бы оттягивает от атомов водорода связывающие электроны. В результате создания такой образуется диполь. Кислородный атом приобретает не очень большой заряд отрицательный, а водородные атомы - небольшой положительный заряд, который притягивается к электронам (их неподеленной паре) на кислородном атоме соседней молекулы Н2О (то есть воды). Таким образом, можно сказать, что водородная связь - это образующаяся между водородным атомом и электроотрицательным атомом. Важной особенностью водородного атома является то, что при притяжении его связующих электронов оголяется его ядро (то есть протон, другими электронами не экранированный). И хотя водородная связь более слабее, чем ковалентная, именно она обуславливает целых ряд аномальный свойств Н2О (воды).
Чаще всего эта связь образуется с участием атомов следующих элементов: кислород (О), азот (N) и фтор (F). Это происходит по той причине, что атомы данных элементов имеют малые размеры и характеризуются высокой электроотрицательностью. С атомами размера большего (сера S или хлор Cl) образующаяся водородная связь слабее, несмотря на то, что по своей электроотрицательности эти элементы сравнимы с N (то есть с азотом).
Существует два типа водородной связи:
1. Водородная межмолекулярная связь
- появляется между двумя молекулами, например: метанол, аммиак, фтороводород.
2. Водородная связь внутримолекулярная
- появляется внутри одной молекулы, например: 2-нитрофенол.
Также в настоящее время есть мнение, что водородная бывает слабой и сильной. Они отличаются друг от друга по энергии и длине связи (расстояние между атомами):
1. Водородные связи слабые. Энергия - 10-30 кДж/моль, длина связи - 30. Все вещества, перечисленные выше, являются примерами нормальной или слабой водородной связи.
2. Водородные связи сильные. Энергия - 400 кДж/моль, длина - 23-24. Данные, полученные экспериментальным путем, свидетельствуют о том, что сильные связи образуются в следующих ионах: ион-водороддифторид -, ион-гидратированный гидроксид -, ион оксония гидратированный +, а также в различных других органических и неорганических соединениях.
Влияние водородных межмолекулярных связей
Аномальные значения и плавления, энтальпии испарения и некоторых соединений можно объяснить наличием связей водородных. Вода имеет аномальные значения всех перечисленных свойств, а фтороводород и аммиак - температуры кипения и плавления. Вода и фтороводород в твердом и жидком состояниях из-за наличия в них водородных межмолекулярных связей считаются полимеризованными. Данная связь объясняет не только слишком высокую температуру плавления данных веществ, но также и их малую плотность. Причем при плавлении водородная связь частично разрушается, из-за чего молекулы воды (Н2О) упаковываются более плотно.
Димеризацию некоторых веществ например, бензойная и уксусная) можно также объяснить наличием в них связи водородной. Димер - это две молекулы, которые связаны между собой. По этой причине температура кипения карбоновых кислот выше, чем у соединений, имеющих приблизительно такую же Например, у кислоты уксусной (СН3СООН) температура кипения равна 391 К, в то время как у ацетона (СН3СОСН3) она равна 329 К.
Влияние водородных внутримолекулярных связей
Эта связь тоже влияет на структуру и свойства различных соединений, таких как: 2- и 4-нитрофенол. Но наиболее известный и важный пример водородной связи - это дезоксирибонуклеиновая кислота (сокр.: ДНК). Молекулы этой кислоты свернуты в виде двойной спирали, две нити которой соединены между собой водородной связью.
Гидрогенная связь - образовывается между «+» заряженными атомами водорода и «-» заряженными атомами других молекул.
Очень часто эта взаимосвязь возникает и существует из-за взаимодействия атома водорода с такими атомами: оксиген (О), нитроген (N). Это происходит вследствие того, что данные элементы имеют небольшой удельный вес и характеризуются высокой электроотрицательностью. Элементы, которые имеют больший удельный вес - сера S или хлор Cl-связываются с водородом менее прочно, хотя их электроотрицательность сравнима с нитрогеном.
Вконтакте
Типы гидрогенной связи
- Межмолекулярная водородная - возникает между двумя элементами, пример: метиловый спирт.
- Водородная (гидрогенная) внутримолекулярная - образуется внутри элемента, пример: 2-нитрофенол.
Межмолекулярная гидрогенная связь
 Совместная электронная пара смещается от атома водорода к отрицательно заряженному атому. При этом водород входит в комплекс с неразделенной электронной парой другого атома или иона.
Совместная электронная пара смещается от атома водорода к отрицательно заряженному атому. При этом водород входит в комплекс с неразделенной электронной парой другого атома или иона.
Н-связь графически изображают в виде точек, тем самым показывая, что она слабее ковалентной (примерно в 10−15 раз).
Молекулы воды (две) и молекулы уксусной кислоты (две)
Внутримолекулярная гидрогенная взаимосвязь . Ей свойственно находиться в таких структурах, как многоатомные спирты, углеводы, белки.
Молекула салициловой кислоты
Химические взаимодействия делятся на слабые и сильные. Их отличие состоит в том, что при разрыве они выделяют разную энергию и у них различные по длине (расстояние между атомами):
1. Слабые. Содержание энергии - 15−25 кдж/моль, длина равна 30.
2. Сильные. Энергия - 300 кдж/моль, длина 22−23.
Для образования Н-св. характерно два типа отдачи ионов - электростатический и донорно - акцепторный. Интересно то, что донором выступает более сильный элемент (F, O, N), а акцептором - атом водорода.
Механизм образования водородной связи
Хорошо разбирать механизм образования водородной связи на примере её между молекулами воды. Н-св. на рисунках обозначается 3 точками. Атом гидрогена имеет всего лишь один электрон, который при взаимодействии с атомом большей электроотрицательности может условно оголять ядро, что, в свою очередь, образует дополнительную взаимосвязь с другим атомом. Это и есть водородная связь.
Вода — это вещество, между молекулами которого образуются водородные связи.

Кластеры из нескольких молекул воды
Благодаря водородным взаимосвязям молекулы воды взаимодействуют друг с другом, что приводит к образованию кластеров или комплексов воды. Одним из ярких примеров является димер воды.
Н-св. считаются довольно слабыми и неустойчивыми: считается, что они легко возникают, но и также легко разрушаются. Для водородных связей характерен симптом тепловой флюктуации. Вода представляет собой сеть из молекул, связанных водородными связями.
Аномальные свойства, обеспеченные водородной взаимосвязью
 Молекула воды состоит из трёх молекул и содержит 4 Н-св. Здесь присутствуют 2 атома водорода, а кислород, имея две неподеленные электронные пары, связывается с атомами Н ближайших молекул Н2О.
Молекула воды состоит из трёх молекул и содержит 4 Н-св. Здесь присутствуют 2 атома водорода, а кислород, имея две неподеленные электронные пары, связывается с атомами Н ближайших молекул Н2О.
Н-св. обеспечивают высокие температуры кипения и плавления. Без них эти показатели были бы намного меньше.
Н-св. в молекулах воды обладают достаточной силой и препятствуют её плавлению и испарению.
А также они обеспечивают ещё одно свойство Н2О, которое характеризуется тем, что при плавлении воды её плотность повышается.
Наибольшее значение имеет плотность воды (1,00 г/мл) при температуре 4 градуса Цельсия. Эта температура характерна для зимнего времени и находится на дне пресных водоёмов, там же и находится вода с максимальной плотностью.
Как изменяются свойства веществ в зависимости от водородной связи
Наиболее достоверным признаком наличия в веществе межмолекулярной Н-св. является показатель кипения вещества. Одна из высоких температур кипения у воды (100 o C так как для того чтобы разрушить межмолекулярные связи в H2O нужно затратить больше энергии). Н-св. сильно может влиять на физические и химические свойства вещества. Межмолекулярная связь обеспечивает повышение температуры плавления и кипения различных веществ. Вещества, которые содержат ОН-группы -моносахариды, дисахариды, как правило, обладают отличной гидрофильностью.
